
Arzneimittel zur Behandlung von Krebs - eine Übersicht
BlogTesaser_Stand
Alle von der Europäischen Kommission zugelassenen Medikamente zur Behandlung von Krebs in Wirkstoffklassen basierend auf ihrem Wirkungsmechanismen und ihren molekularen pharmakologischen Zielen
Heute sind Krebsmedikamente mit fast 200 verschiedenen Wirkstoffen und mehr als 70 verschiedenen molekularen Zielen oder pharmakologischen Mechanismen über das zentralisierte Verfahren (CP) der Europäischen Arzneimittel-Agentur (EMA) zugelassen worden. Basierend auf ihren molekularen Zielen und pharmakologischen Mechanismen werden die Medikamente in verschiedene Klassen und Gruppen verwandter Klassen eingeteilt.
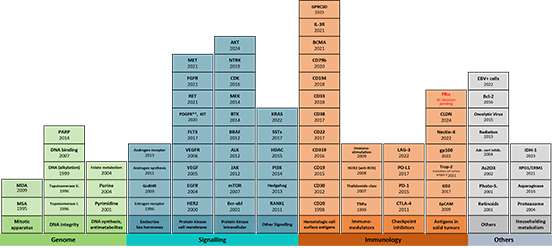
Legende Abbildung 1: Übersicht über Wirkungsmechanismen und pharmakologischen Ziele der in der EU zentralisiert zugelassenen Arzneimittel zur Behandlung von Krebs. Unterschieden werden drei Ebenen: die Klasse (die einzelnen Boxen), die Gruppe (die einzelne Säule aus übereinander gestellten Boxen) und die farblich gekennzeichneten vier Kategorien: (1) mit der Wirkung auf das Genom (grün) oder (2) mit der Wirkung auf intra- und extrazelluläre Signalübertragung (blau), (3) mit der Wirkung durch immunologische Mechanismen (orange) und (4) Wirkstoffe, mit keiner dieser Kategorien zugehörigen Mechanismen (grau). Für jede Klasse ist das Datum der europäischen Zulassung der ersten Substanz dieser Klasse und das molekulare Ziel oder der Wirkungsmechanismus angegeben (siehe Abkürzungen). Quelle d. Abbildung aus ERON-S1-24, modifiziert.
Wirkstoffe mit demselben molekularen Ziel oder pharmakologischen Mechanismus bilden eine Klasse. Dabei definieren das molekulare Ziel und die pharmakologische Wirkung die Klasse, unabhängig davon, ob verschiedene Substanzen unterschiedlich mit demselben Ziel interagieren. Beispielsweise werden Antikörper, die die Aktivität einer Rezeptortyrosinkinase hemmen, in dieselbe Klasse wie niedermolekulare Arzneimittel eingeordnet, die die Aktivität desselben Ziels hemmen und Antikörper gegen CD19 gehören danach in dieselbe Klasse wie CAR-T Zellen gegen CD19. Antikörper-Wirkstoff-Konjugate werden derselben Klasse zugeordnet wie der ursprüngliche (nicht konjugierte) Antikörper, selbst wenn eine zusätzliche zytotoxische Wirkung des Konjugats offensichtlich ist. Ebenso werden bispezifische T-Zell-Engager derselben Klasse zugeordnet wie einfache Antikörper mit demselben molekularen Ziel.
Klassen mit ähnlichen molekularen Zielen oder Wirkungsmechanismen werden zu Gruppen zusammengefasst, und als übergreifende Struktur unterscheiden wir Kategorien, die auf dem allgemeinen Prinzip der pharmakologischen Wirkung basieren: Wirkung auf das Genom, die Signalübertragung oder auf oder durch das Immunsystem. In Abbildung 1 werden die einzelnen Klassen als Boxen und die Gruppen als Säulen aus den Boxen dargestellt, während die Kategorien an der Farbe unterschieden werden.
Medikamente, die auf das Immunsystem oder über immunologische Mechanismen wirken, fallen in die Kategorie "Immunologie" (Immunolgy). Arzneimittel, die auf die DNA oder DNA-Prozesse wie Synthese oder Replikation, DNA-Integrität oder Mitose wirken, werden in die Kategorie "Genom" (Genome) eingeordnet. Arzneimittel, die in Signalwege wie endokrine Signalwege oder Proteinkinasekaskaden eingreifen, fallen in die Kategorie "Signalübertragung" (Signaling). Andere Produkte, die keiner dieser Kategorien zugeordnet werden können und (noch) kein einheitliches pharmakologisches Wirkprinzip aufweisen, werden als "Sonstige" (Others) zusammengefasst.
Die hohe Anzahl und Heterogenität der Zielstrukturen zeigt, wie stark sich das Instrumentarium für die pharmakologische Behandlung von Krebs in den letzten zwei Jahrzehnten erweitert hat. Gleichzeitig gab es offensichtlich Verschiebungen bei den bevorzugten pharmakologischen Mechanismen oder molekularen Zielen von Krebsmedikamenten. In den letzten Jahren gab es vor allem im Bereich der Immuntherapie und der Zellsignale entscheidende neue Entwicklungen – während mit den Poly-ADP-Ribose-Polymerase Hemmern die letzte neue Klasse in der Kategorie "Genom" schon vor 10 Jahren eingeführt wurde.
Kategorie Immunologie
Während die Krebsimmuntherapie derzeit das aktivste und interessanteste Feld ist, ist es auch bemerkenswert, wie lange der Ansatz einer immunologischen Krebstherapie bereits verfolgt wird. Coleys Toxine sind wahrscheinlich das bekannteste frühe Beispiel. Ende des 19. Jahrhunderts stimulierte William B. Coley das Immunsystem von Sarkompatienten mit bakteriellen Toxinen. Obwohl es hundert Jahre später war, dass die Krebsimmuntherapie an Fahrt gewann, gilt William B. Coley allgemein als der Vater der Krebsimmuntherapie. Doch selbst William B. Coley hatte Vorläufer: Es wird angenommen, dass seine Forschung auf der Arbeit von Friedrich Fehleisen aufbaute – und dass Fehleisen experimentelle Ansätze von Wilhelm Busch (Bonn) aufgenommen hatte. Es ist daher verlockend zu folgern, dass zwar nicht der Vater, aber der Großvater der Krebsimmuntherapie in Bonn wirkte.
Die Kategorie „Immunology“ umfasst vier Gruppen pharmakologischer Klassen: hämatologische Zelloberflächenantigene, Immunmodulatoren, Checkpoint-Inhibitoren und Antigene in soliden Tumoren. Dabei sind zwei Gruppen besonders hervorzuheben: Erstens die Gruppe der Immun-Checkpoint-Inhibitoren mit ihrer sehr hohen klinischen Relevanz und ihrem breiten Einsatzspektrum gegen eine Vielzahl verschiedener Tumore und zweitens die Gruppe der Substanzen, die auf hämatologische Zelloberflächenantigene abzielen, der höchste "Turm" mit der größten Anzahl verschiedener molekularer Zielstrukturen. Mehr als die Hälfte aller innovativen neuen Wirkstoffe oder innovativen Produkte in der Kategorie Immunologie fallen in diese Gruppe. Während die Produkte in der Gruppe "Hämatologische Zelloberflächenantigene" in der Regel enge, Zelltyp-spezifische, meist seltene Indikationen haben, sind Checkpoint-Inhibitoren nicht von Natur aus tumortypspezifisch. Sie "entblocken" das Immunsystem und können gegen eine Vielzahl verschiedener Tumore eingesetzt werden. Dementsprechend sehen wir ein sehr hohes Maß an Aktivitäten nach der Zulassung zur Erweiterung der Indikation für diese Medikamente, bei einigen Produkten mit neuen Indikationen alle paar Monate.
Vergleichsweise wenig neue Entwicklungen finden sich in der Gruppe der Immunmodulatoren, deren klinische Verwendung, mit Ausnahme der Wirkstoffe der Thalidomid-Klasse, gegenwärtig eher begrenzt erscheint.
Im Gegensatz zur erfolgreichen Entwicklung von Krebsimmuntherapien, die auf hämatologische Zelloberflächenantigene abzielen, werden Antigene von soliden Tumoren seltener als Ziele für die Immuntherapie verwendet. Bei Karzinomen sind tumorspezifische Antigene (oder zumindest im Tumor deutlich stärker als in normalen Zellen exprimierte Antigene) für eine gezielte Therapie notwendig. Dies ist bei Leukämien und Lymphomen nicht nötig, hier reichen Zelltyp-spezifische Antigene aus. Bei diesen Erkrankungen ist es akzeptabel sowohl die Krebszellen als auch die zugehörigen normalen, nicht neoplastischen Zellen möglichst vollständig zu eliminieren, da trotzdem eine Regeneration möglich ist - sofern die Stammzellen, die das Zelltyp-spezifische Antigen nicht exprimieren, erhalten bleiben.
In Tabelle 1 sind alle Wirkstoffe der Kategorie Immunologie aufgeführt, die im zentralisierten Verfahren der EMA zugelassen wurden und noch auf dem Markt sind.

Legende Tabelle 1: Immuntherapeutika zur Behandlung von Krebs: Name des Arzneimittels, Name der Wirksubstanz, Jahr der Zulassung in der EU. *Zulassung vom CHMP empfohlen, Entscheidung der europäischen Kommission ausstehend.
Kategorie Signalübertragung
Die Zellsignalisierung ist die Kategorie mit den meisten Produkten oder Wirkstoffen, mit der größten Anzahl unterschiedlicher Wirkmechanismen oder molekularer pharmakologischer Zielstrukturen. Dabei ist das Prinzip, den Empfang oder die Übertragung von Wachstumssignalen zu unterbrechen oder zu modulieren, vergleichsweise alt: Bereits 1896 empfiehlt Beatson Oophorektomie bei Brustkrebs in seinem Artikel “On Treatment of Inoperable Cases of Carcinoma of the Mamma: Suggestions for a New Method of Treatment, with Illustrative Cases” in den Transactions of the Medico-Chirurgical Society of Edinburgh. Erstaunlicherweise dauerte es fast ein halbes Jahrhundert, bis ein vergleichbarer chirurgischer Ansatz zur Behandlung des Prostatakarzinoms bei Männern aufgenommen wurde.
In der Folge und als Alternative zur Kastration wurden Medikamente für die endokrine Behandlung von Krebs wurden entwickelt, lange bevor die Signalübertragung im Sinne des „cell signaling“ als Wirkprinzip vieler Krebsarzneimittel in den Vordergrund trat. Viele der endokrinologisch wirkenden Arzneimittel wurden bereits im letzten Jahrhundert von nationalen Regulierungsbehörden zugelassen, weshalb nur einige davon in der Liste der im zentralisierten Verfahren der EU zugelassenen Medikamente zur Behandlung von Krebs aufgeführt sind.

Legende Tabelle 2: Arzneimittel zur Behandlung von Krebs, die intra- oder extrazelluläre Signalwege als pharmakologisches Ziel haben: Name des Arzneimittels, Name der Wirksubstanz, Jahr der Zulassung in der EU.
Innerhalb der Kategorie Signalübertragung ist die Gruppe der Proteinkinase-Inhibitoren die bei weitem größte und wichtigste. Je nach Zielort, d. h. ob intrazellulär oder membrangebunden mit einem extrazellulären Teil, können zwei Gruppen unterschieden werden. Während intrazelluläre Proteinkinasen für Antikörper nicht zugänglich sind, kann eine große Anzahl verschiedener Krebsmedikamente, darunter kleine Moleküle und monoklonale Antikörper, zur Hemmung von zellmembrangebundenen Proteinkinasen eingesetzt werden. Häufig ist derselbe Rezeptor die pharmakologische Zielstruktur für mehrere verschiedene Wirkstoffe. So richten sich beispielsweise mehr als zehn verschiedene Wirkstoffe gegen den VEGFR, den Rezeptor für VEGF* (vaskulären endothelialen Wachstumsfaktor, englisch vascular endothelial growth factor).
Eine weitere Gruppe besteht aus Substanzen, die zumeist intrazelluläre Signalwege als pharmakologisches Ziel haben, die aber weder durch die Hemmung von Proteinkinasen noch der Signalübertragung durch Sexualhormonen wirken. In Tabelle 2 sind alle Wirkstoffe der Kategorie "Signalübertragung" aufgeführt, die mit dem zentralisierten Verfahren der EMA zugelassen wurden und noch auf dem Markt sind.
Kategorie "Genom"
Die ersten Wirkstoffe dieser Gruppe wurden bereits zur Zeit des Zweiten Weltkriegs aus chemischen Kampfstoffen abgeleitet. In den 1940er Jahren entwickelten Gilman und Goodman die ersten modernen Chemotherapeutika aus Senfgas und auch heute noch gehören Substanzen dieser Klasse zum Standardrepertoire der Chemotherapie. Viele dieser Produkte wurden in nationalen Verfahren zugelassen, lange bevor die EMA gegründet und das zentralisierte europäische Verfahren für innovative Krebsmedikamente verpflichtend wurde. Deshalb ist die hier vorliegende Sammlung von Klassen im Gegensatz zu den anderen Kategorien eher unvollständig. Tabelle 3 listet alle Wirkstoffe auf, die im zentralisierten Verfahren der EMA zugelassen wurden und noch auf dem Markt sind.

Legende Tabelle 3: Arzneimittel zur Behandlung von Krebs, die das Genome der Krebszellen als pharmakologisches Ziel haben. Name des Arzneimittels, Name der Wirksubstanz, Jahr der Zulassung in der EU. Zahlreiche Arzneimittel mit diesem Wirkungsmechanismus wurden lange vor Gründung der EMA durch nationale Zulassungsverfahren eingeführt. In dieser Übersicht sind nur die im zentralisierten Verfahren der EMA zugelassenen Arzneimittel dargestellt.
Kategorie "Sonstiges"
Arzneimittel, die in der EU für die Behandlung von Krebs zugelassen sind und keiner der vorgenannten Kategorien zugeordnet werden können, wurden in die Kategorie „others“ (Sonstige) eingeordnet. Es ist erstaunlich, wie weit einige der therapeutischen Ansätze in dieser Gruppe in die Vergangenheit zurückreichen. Die ersten dokumentierten Versuche, Krebspatienten mit Arsen zu behandeln, reichen über 200 Jahre zurück. Damals wurde Arsen, im Gegensatz zur heutigen Verwendung zur Behandlung der Promyelozytenleukämie, nicht zur Behandlung der Krebserkrankung, sondern offensichtlich als Schmerzmittel gegeben. Dies erklärt auch den auf den ersten Blick befremdlichen Satz: „Dieser Fall erwies sich, wie zu erwarten war, als tödlich, aber das Heilmittel enttäuschte meine Erwartung nicht“. Auch die Strahlentherapie von Tumoren reicht weit zurück. Die ersten Veröffentlichungen zur Strahlentherapie von Tumoren sind fast 100 Jahre alt. Am Rande bemerkenswert scheint, dass bereits damals neue Therapieansätze häufig zuerst in den USA eingeführt wurden – wie auch heute viele innovative Medikamente zuerst in den USA verfügbar werden.

Legende Abbildung 2: Frühe Berichte über heute im zentralisierten Verfahren der EMA zugelassene Wirkstoffe zur Behandlung von Krebs. Radium ist als Xofigo®seit 2013 und Arsen als Trisenox® seit 2002 zugelassen.
Das breite Spektrum der Wirkstoffe in dieser Gruppe ist bemerkenswert ist die große Heterogenität dieser Gruppe „Sonstige“. Neben diesen historisch alten und chemisch einfachen Wirkstoffen wie Arsen oder Radium haben wir in dieser Kategorie moderne, komplexe therapeutische Ansätze wie onkolytische Viren oder Zelltherapie. Gemeinsamkeiten sind möglicherweise erkennbar für eine Gruppe von Wirkstoffen, deren pharmakologischen Wirkung auf bestimmte Abschnitte des normalen Zellstoffwechsel gerichtet ist, wenn diese Stoffwechselwege von besonderer Bedeutung für Krebszellen sind.
Tabelle 4 listet alle Wirkstoffe auf, die im zentralisierten Verfahren der EMA zugelassen wurden und noch auf dem Markt sind.

Legende Tabelle 4: Arzneimittel zur Behandlung von Krebs, die nicht den Kategorien in Tabellen 1-3 zugeordnet werden können. Name des Arzneimittels, Name der Wirksubstanz, Jahr der Zulassung in der EU.
Diese Übersicht entspricht dem Stand vom November 2024.
